Lorsqu’un antigène pénètre dans l’organisme, le système immunitaire réagit au départ en déclenchant une réponse immunitaire innée. Au cours de cette réponse immunitaire, on assiste à la migration des leucocytes depuis le flux sanguin vers le foyer de l’infection, grâce à l’action essentielle de ce que l’on appelle les molécules d’adhésion. Parmi ces molécules, on trouve la famille des intégrines et des sélectines, une classe de protéines impliquées dans l’adhésion/union des leucocytes à l’endothélium vasculaire.
Les syndromes de déficit d’adhésion leucocytaire (DAL) constituent un type d’immunodéficience qui peut provoquer divers problèmes lors du déclenchement de la réponse immunitaire, principalement face à des bactéries et d’autres micro-organismes, ce qui met notre santé en péril. On peut distinguer principalement deux types de DAL, le DAL-1 et le DAL-2.
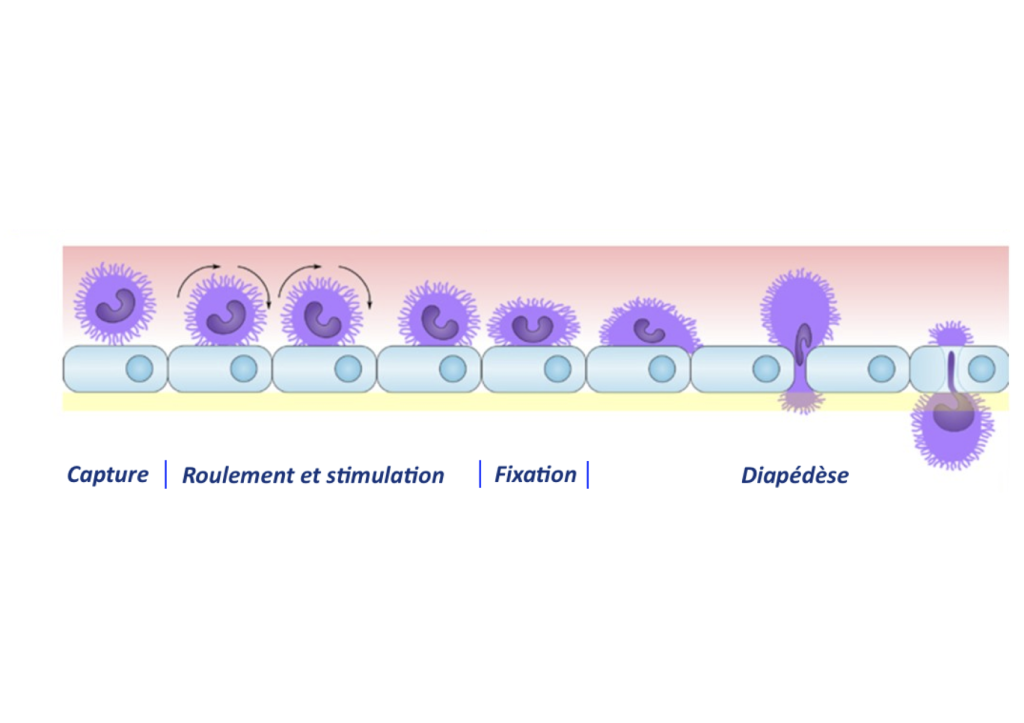
Étapes de la migration leucocytaire
- Capture : Lors de cette étape, on assiste à une liaison faible entre le leucocytes et l’endothélium via les sélectines et leurs ligands, qui sont indispensables lors de cette phase. La E-sélectine, spécifique à l’endothélium, est exprimée uniquement dans les cas d’infection ou d’inflammation, puisque le but est que les leucocytes ne soient retenus que lorsqu’ils doivent sortir spécifiquement du vaisseau sanguin.1
- Stimulation : Dans le tissu infecté, des cytokines chimiotactiques (chimiokines) sont synthétisées : elles vont chercher à attirer le leucocyte vers le foyer de l’infection. Ces cytokines stimulent également l’activation par le leucocyte des intégrines présentes à sa surface.
- Fixation : Les intégrines exprimées par le leucocyte se lient à leurs récepteurs de l’endothélium, ce qui crée des liaisons plus fortes et stabilise la cellule.
- Diapédèse : C’est le processus de migration des leucocytes à travers les parois des vaisseaux pour qu’ils puissent rejoindre le foyer de l’infection en suivant la piste des chimiokines.
Syndromes de déficit d’adhésion leucocytaire
Comme on l’a expliqué plus tôt, il existe deux types de DAL, selon la molécule affectée :
Le DAL-1 se produit suite à la mutation du gène qui code pour la protéine CD18, qui fait partie de la famille des intégrines. La mutation de cette protéine entraîne l’altération de toutes les fonctions qui dépendent des processus d’adhésion cellulaire, comme la phase de fixation ou la diapédèse. La maladie peut être modérée ou grave selon le degré d’expression (léger ou nul) de la protéine. Les manifestations cliniques s’observent en général au cours des deux premières années de vie et prennent la forme d’infections bactériennes récurrentes.2
Dans le cas du DAL-2, les niveaux de la protéine CD18 sont normaux, mais on remarque une expression défectueuse d’un ligand de diverses molécules d’adhésion, à la fois des sélectines et des intégrines.3 Cela perturbe les fonctions de « capture » des leucocytes par l’endothélium. C’est un syndrome assez rare. Les infections modérées sont fréquentes, la parodontite chronique étant le seul symptôme persistant.
Référence de l’image:
Shèmas modifié à partir du fichier, qui se trouve sous la lisence Creative Commons Attribution 3.0 Unported, y créé d’après un dessin de: U. H. von Andrian et C. R. Mackay : T-Cell Function and Migration. NEJM. 2000, p. 1025 ; et K. Ley et al. : Getting to the site of inflammation : the leukocyte adhesion cascade updated. dans : Nature Reviews Immunology 7, 2007, p. 679.
Bibliographie
- Barreiro, Olga, and Francisco Sánchez-Madrid. « Molecular basis of leukocyte–endothelium interactions during the inflammatory response. » Revista Española de Cardiología (English Edition) 62.5 (2009): 552-562.
- Etzioni, Amos, et al. « Recurrent severe infections caused by a novel leukocyte adhesion deficiency. » New England Journal of Medicine 327.25 (1992): 1789-1792.
- Karsan, Aly, et al. « Leukocyte Adhesion Deficiency Type II is a generalized defect of de novo GDP-fucose biosynthesis. Endothelial cell fucosylation is not required for neutrophil rolling on human nonlymphoid endothelium. » Journal of Clinical Investigation 101.11 (1998): 2438.